تایید داروی ترکیبی Niraparib و Abirateron Acetate برای درمان سرطان پروستات
سازمان غذا و داروی ایالات متحده (FDA)، برای داروی ترکیبی نیراپاریب و ابیراترون استات در درمان سرطان پروستات مقاوم به اختگی متاستاتیک که رو به وخامت میرود، تاییدیه صادر کرد. این دارو که به صورت یک بار در روز مصرف میشود، اولین و تنها درمان خوراکی است که ترکیبی از مهارکننده PARP نیراپاریب با آبیراترون استات را همزمان به بدن بیمار میرساند.
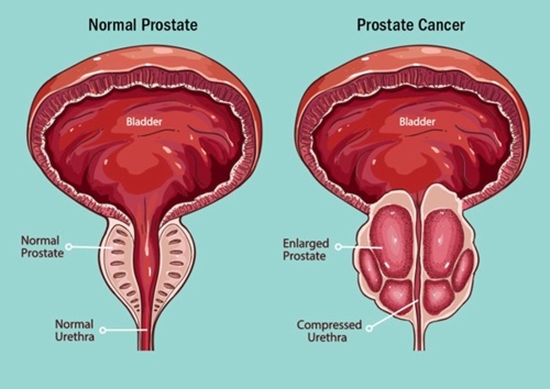
سازمان غذا و داروی ایالات متحده (FDA)، برای داروی ترکیبی نیراپاریب و ابیراترون استات در درمان سرطان پروستات مقاوم به اختگی[1] متاستاتیک که رو به وخامت میرود، تاییدیه صادر کرد. این دارو که به صورت یک بار در روز مصرف میشود، اولین و تنها درمان خوراکی است که ترکیبی از مهارکننده PARP نیراپاریب با آبیراترون استات را همزمان به بدن بیمار میرساند.

تایید FDA بر اساس یافتههای مطالعه پزشکی دقیق MAGNITUDE فاز 3، یک کارآزمایی تصادفیسازی شده و کنترلشده با دارونما با 423 بیمار، که 225 نفر (53%) دارای جهشهای ژن BRCA بودند، با استفاده از روش بافتی مانند FoundationOne CDx تعیین شد.
در میان زیرگروههای دارای جهش BRCA، بقای بدون پیشرفت رادیوگرافی 16.6 ماه در مقابل 10.9 ماه بود (نسبت خطر [HR]، 0.53؛ فاصله اطمینان 95% [CI]، 0.36 - 0.79؛ P = 0.0014). در این زیر گروه، یک تجزیه و تحلیل کلی بقای اکتشافی میانگین 30.4 ماه در مقابل 28.6 ماه (HR، 0.79؛ 95% فاصله اطمینان (CI، 0.55 - 1.12) را نشان داد، که به نفع بازوی درمان است.
اگرچه گروه کلی (کسانی که دارای جهش BRCA و بدون آن) بهبود قابل توجهی را در بقای بدون پیشرفت رادیوگرافی نشان دادند، زیر گروه با جهشهای ترمیم نوترکیبی همولوگ غیر BRCA بهبود قابلتوجهی در بقای بدون پیشرفت رادیوگرافی نشان ندادند، که نشان میدهد طبق گفته FDA، مزایای مشاهده شده "در درجه اول" به نتایج در زیر گروه بیماران مبتلا به جهش BRCA نسبت داده شد.
مشخصات ایمنی niraparib و abiraterone acetate به اضافه پردنیزون با مشخصات ایمنی شناخته شده هر تک درمانی مورد تایید FDA مطابقت داشت. عوارض جانبی جدی در 41 درصد از بیماران در بازوی درمان رخ داد. اینها اغلب شامل درد اسکلتی عضلانی (44٪ در مقابل 42٪)، خستگی (43٪ در مقابل 30٪)، یبوست (34٪ در مقابل 20٪)، فشار خون بالا (33٪ در مقابل 27٪)، و تهوع (33٪ در مقابل 21٪) بود. .
یک واکنش نامطلوب منجر به قطع دائم درمان در 15٪ از بیماران شد.
محقق اصلی کیم چی، MD، در بیانیه مطبوعاتی Janssen اظهار داشت: به عنوان یک پزشک، شناسایی بیمارانی که پیش آگهی بدتری دارند، به ویژه کسانی که سرطان آنها دارای جهش BRCA است، اولویت دارد. ما مطالعه MAGNITUDE را برای شناسایی زیرمجموعه بیمارانی که به احتمال زیاد از درمان هدفمند با AKEEGA بهره مند می شوند را طراحی کردیم و به ما کمک کرد تا بفهمیم چگونه می توانیم به طور بالقوه به نتایج سلامت بهتری برای بیماران دست یابیم.
حدود 10 تا 15 درصد از بیمارانی که به سرطان پروستات مقاوم به اختگی متاستاتیک مبتلا میشوند، تغییرات ژن BRCA دارند و این بیماران احتمال ابتلا به بیماریهای تهاجمی، نتایج ضعیف و بقای کوتاهتری دارند. شلبی مونیر، معاون برنامههای آموزشی و آموزشی بیماران در ZERO Cancer Prostate، گفت: بنابراین، این عامل جدید "یک گزینه درمانی مهم برای بیماران مبتلا به سرطان پروستات به ارمغان میآورد، زیرا آنها مسیر خود را در پیش میبینند."
اطلاعات تجویز دوز توصیه شده 200 میلی گرم نیراپاریب و 1000 میلی گرم آبیراترون را یک بار در روز همراه با 10 میلی گرم پردنیزون در روز تا پیشرفت بیماری یا مسمومیت غیرقابل قبول فهرست می کند. بیماران همچنین باید یک آنالوگ هورمون آزاد کننده گنادوتروپین را به طور همزمان دریافت کنند یا باید ارکیکتومی دوطرفه داشته باشند.
11 آگوست 2023


ارسال نظر